检测到您当前使用浏览器版本过于老旧,会导致无法正常浏览网站;请您使用电脑里的其他浏览器如:360、QQ、搜狗浏览器的极速模式浏览,或者使用谷歌、火狐等浏览器。
 下载Firefox
下载Firefox
检测到您当前使用浏览器版本过于老旧,会导致无法正常浏览网站;请您使用电脑里的其他浏览器如:360、QQ、搜狗浏览器的极速模式浏览,或者使用谷歌、火狐等浏览器。
 下载Firefox
下载Firefox
近日Cancer Research期刊在线发表了郑晓峰研究组的题为“SENP1 decreases RNF168 phase separation to promote DNA damage repair and drug resistance in colon cancer”的研究文章。该研究发现去SUMO化酶SENP1应答DNA双链断裂损伤被招募到损伤位点,通过去除RNF168的SUMO化修饰来破坏其诱导的RNF168液-液相分离,进而促进非同源末端连接修复,证实SENP1在结肠癌细胞中高表达,促进癌细胞对化疗药物的耐受。该研究揭示了SUMO化修饰通过影响液-液相分离调控DNA损伤修复效率及肿瘤细胞耐药的分子机制。
DNA作为遗传信息的主要载体,其结构的完整与功能的完善对于维持基因组的稳定性和保障生命体正常生理活动具有重要意义。不同类型的DNA损伤修复对于维持基因组稳定性至关重要,针对最严重的DNA双链断裂损伤(DSB),细胞主要通过非同源末端连接修复(NHEJ)与同源末端重组修复(HR)进行修复。泛素E3连接酶RNF168是DNA双链断裂损伤修复通路中早期响应损伤的修复蛋白。已有的研究表明,蛋白质翻译后修饰在双链断裂修复中发挥重要的调控作用,但是RNF168的翻译后修饰在其功能中的调控作用有待于揭示。
该研究发现RNF168的SUMO化修饰促进其在细胞核内液-液相分离(LLPS)的形成,阻碍RNF168被招募到DNA损伤位点,进而下调RNF168对组蛋白H2A的泛素化修饰。同时,该LLPS液滴包裹下游关键修复蛋白53BP1,抑制其被招募到损伤修复位点并最终导致NHEJ修复效率的下降。进一步研究表明,SENP1是RNF168的特异性去SUMO化酶。当DNA双链断裂损伤发生时,结肠癌细胞中高表达的SENP1去除RNF168的SUMO化修饰,阻止RNF168液-液相分离形成,从而维持基因组的稳定性,使肿瘤细胞对化疗药物产生抵抗,最终导致肿瘤进一步恶化,肿瘤组织中SENP1的高水平表达与癌症患者预后不良相关。
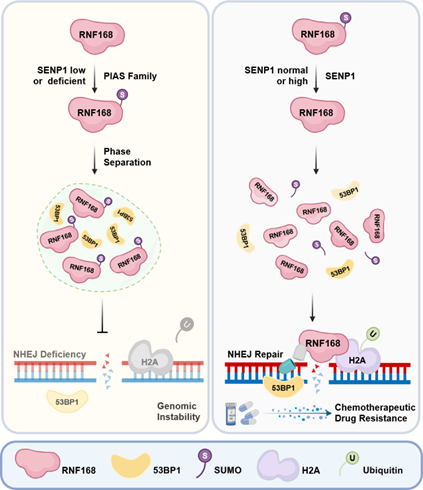
SENP1调控DNA损伤修复模式图
该研究利用癌细胞和小鼠模型,揭示了RNF168 SUMO化修饰通过液-液相分离调控DNA损伤应答的分子机制,证明SENP1-RNF168-53BP1信号轴在肿瘤细胞的化疗耐药性中发挥重要调控作用,提示抑制SENP1是一种潜在的结肠癌治疗策略。
北京大学郑晓峰课题组的博士研究生卫敏为文章的第一作者,黄新平、廖礼铭也在该论文中做出了重要贡献。郑晓峰教授为文章的通讯作者。该研究得到了国家自然科学基金重点项目、蛋白质与植物基因研究国家重点实验室、金沙集团wwW3354CC、金沙集团wwW3354CC仪器中心以及凤凰平台的大力支持。